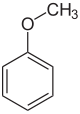
Anisol - Anisole
|
|
|||

|
|||
| Jména | |||
|---|---|---|---|
|
Název IUPAC
Methoxybenzen
|
|||
|
Preferovaný název IUPAC
Anisol |
|||
| Ostatní jména
Methyl fenyl ether
Phenoxymethane |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| 506892 | |||
| ČEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Informační karta ECHA |
100,002,615 |
||
| Číslo ES | |||
| 2964 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
| UN číslo | 2222 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| C 7 H 8 O | |||
| Molární hmotnost | 108,140 g · mol −1 | ||
| Vzhled | Bezbarvá kapalina | ||
| Hustota | 0,995 g / cm 3 | ||
| Bod tání | -37 ° C (-35 ° F; 236 K) | ||
| Bod varu | 154 ° C (309 ° F; 427 K) | ||
| Rozpustnost | Nerozpustný | ||
| -72,79 · 10 −6 cm 3 /mol | |||
| Nebezpečí | |||
| Piktogramy GHS |
 
|
||
| Signální slovo GHS | Varování | ||
| H226 , H315 , H319 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P264 , P280 , P302+352 , P303+361+353 , P305+351+338 , P321 , P332+313 , P337+313 , P362 , P370+378 , P403+ 235 , P501 | |||
| NFPA 704 (ohnivý diamant) | |||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
|
LD 50 ( střední dávka )
|
3700 mg/kg (krysa, orální) | ||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
Anisol nebo methoxybenzen , je organická sloučenina s vzorcem CH 3 OC 6 H 5 . Je to bezbarvá kapalina s vůní připomínající semínka anýzu a ve skutečnosti se mnoho jejích derivátů nachází v přírodních a umělých vůních. Sloučenina se vyrábí hlavně synteticky a je předchůdcem jiných syntetických sloučenin. Je to ether . Anisole je standardní činidlo praktické i pedagogické hodnoty.
Lze jej připravit Williamsonovou etherovou syntézou ; fenoxid sodný reaguje s methylhalogenidem za vzniku anisolu.
Reaktivita
Anisol prochází elektrofilní aromatickou substituční reakcí vyšší rychlostí než benzen , který zase reaguje rychleji než nitrobenzen . Methoxyskupina je orto/para řídící skupina, což znamená, že v těchto třech místech se přednostně vyskytuje elektrofilní substituce. Zvýšená nukleofilita anisolu vs. benzenu odráží vliv methoxyskupiny , díky čemuž je prsten bohatší na elektrony. Methoxy skupiny silně ovlivňuje pi oblak prstence jako mesomerního elektronový donor, a ještě více, než jako indukční skupinou odebírající elektrony přes elektronegativita z kyslíku . Kvantitativněji řečeno, Hammettova konstanta pro para -substituci anisolu je -0,27.
Anisol , který ilustruje svou nukleofilitu , reaguje s anhydridem kyseliny octové za vzniku 4-methoxyacetofenonu :
- CH 3 OC 6 H 5 + (CH 3 CO) 2 O → CH 3 OC 6 H 4 C (O) CH 3 + CH 3 CO 2 H
Na rozdíl od většiny acetofenonů, ale odrážející vliv methoxyskupiny, prochází methoxyacetofenon druhou acetylací . Bylo prokázáno mnoho souvisejících reakcí. Například P 4 S 10 převádí anisol na Lawessonovo činidlo , [(CH 3 OC 6 H 4 ) PS 2 ] 2 .
Anisol také indikuje prsten bohatý na elektrony a snadno vytváří π-komplexy s karbonyly kovů , např. Cr (η 6- anisol) (CO) 3 .
Etherová vazba je vysoce stabilní, ale methylovou skupinu lze odstranit kyselinou jodovodíkovou :
- CH 3 OC 6 H 5 + HI → HOC 6 H 5 + CH 3 I
Redukce břízy anisolu poskytne 1-methoxycyklohexa-1,4-dien.
Příprava
Anisol je připraven methylací fenoxidu sodného s dimethylsulfátem chlorid nebo methyl:
- 2 C 6 H 5 O - Na + + (CH 3 O) 2 SO 2 → 2 C 6 H 5 OCH 3 + Na 2 SO 4
Aplikace
Anisol je předchůdcem parfémů , feromonů hmyzu a léčiv . Například syntetický anethol je připraven z anisolu.
Bezpečnost
Anisol je relativně netoxický s LD 50 3700 mg/kg u potkanů. Jeho hlavním nebezpečím je hořlavost.
Viz také
- Anethole
- Bromanisol
- Butylovaný hydroxyanisol
- Éter
- Etylfenylether
- Fenol
- 2,4,6-trichloranisol (korkový nátěr)
Reference
-
^ a b c
Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (Modrá kniha) . Cambridge: The Royal Society of Chemistry . 2014. s. 702–703. doi : 10,1039/9781849733069-00648 . ISBN 978-0-85404-182-4.
Anisol, C 6 H 5 -O-CH 3 , je pouze název ve třídě etherů, která je zachována i jako preferovaný název IUPAC a pro použití v běžném nomenklatury. U preferovaných názvů IUPAC není povolena žádná substituce; obecná nomenklatura je za určitých podmínek povolena na kruhu a na postranním řetězci (viz P-34.1.1.4).
- ^ Smith, Michael B .; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6. ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Thomsen, K. Clausen, S. Scheibye, S.-O. Lawesson (1984). „Thiace 2,4-bis (4-methoxyfenyl) -1,3,2,4-dithiadifosfethan 2,4-disulfidem: N-methylthiopyrrolidonem“. Organické syntézy . 62 : 158. doi : 10,15227/orgsyn.062.0158 .Správa CS1: více jmen: seznam autorů ( odkaz )
- ^ E. Peter Kündig (2004). „Syntéza přechodných kovů η 6 -arenových komplexů“. Témata Organomet Chem . 7 : 3–20. doi : 10,1007/b94489 .
- ^ AJ Birch a KB Chamberlain (1977). "Tricarbonyl [(2,3,4,5-η) -2,4-cyklohexadien-1-on] Železo a trikarbonyl [(1,2,3,4,5-η) -2-methoxy-2,4 -Cyklohexadien-1-yl] železo (1+) hexafluorfosfát (1−) z anisolu “. Organické syntézy . 57 : 107. doi : 10,15227/orgsyn.057.0107 .
- ^ GS Hiers a FD Hager (1929). „Anisol“. Organické syntézy . 9 : 12. doi : 10,15227/orgsyn.009,0012 .
- ^ a b Helmut Fiege, Heinz-Werner Voges, Toshikazu Hamamoto, Sumio Umemura, Tadao Iwata, Hisaya Miki, Yasuhiro Fujita, Hans-Josef Buysch, Dorothea Garbe, Wilfried Paulus „Deriváty fenolu“ v Ullmannově encyklopedii průmyslové chemie, 2002, -VCH, Weinheim. doi : 10,1002/14356007.a19_313
- ^ a b MSDS archivováno 1. července 2010 na Wayback Machine
externí odkazy
- Mezinárodní karta chemické bezpečnosti 1014
- Záznam feromonové databáze ferobáz