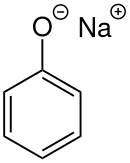
Fenoxid sodný - Sodium phenoxide
|
|
| Jména | |
|---|---|
|
Preferovaný název IUPAC
Fenoxid sodný |
|
| Ostatní jména
Fenolát sodný
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100,004,862 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| C 6 H 5 NaO | |
| Molární hmotnost | 116,09 g/mol |
| Vzhled | Bílá pevná látka |
| Nebezpečí | |
| Hlavní nebezpečí | Škodlivý, žíravý |
| Bod vzplanutí | Nehořlavé |
| Nehořlavé | |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
| Reference na infobox | |
Fenoxid sodný ( fenolát sodný ) je organická sloučenina vzorce NaOC 6 H 5 . Je to bílá krystalická pevná látka. Jeho anion, fenolát, také známý jako fenolát, je konjugovaná báze z fenolu . Používá se jako předzvěst mnoha jiných organických sloučenin, jako je například aryl ethery .
Syntéza a struktura
Nejčastěji se roztoky fenoxidu sodného vyrábějí zpracováním fenolu s hydroxidem sodným. Bezvodé deriváty lze připravit kombinací fenolu a sodíku. Související, aktualizovaný postup používá místo hydroxidu sodného methoxid sodný:
- NaOCH 3 + HOC 6 H 5 → NaOC 6 H 5 + HOCH 3
Struktura
Stejně jako ostatní alkoxidy sodné má pevný fenolát sodný komplexní strukturu zahrnující více vazeb Na-O. Materiál bez rozpouštědel je polymerní, každé centrum Na je vázáno na tři ligandy kyslíku a také na fenylový kruh . Adukty fenoxidu sodného jsou molekulární, jako například kubánový klastr [NaOPh] 4 ( HMPA ) 4 .
Fenoxid sodný může být vyráběn „alkalickou fúzí“ kyseliny benzensulfonové , přičemž jsou sulfonátové skupiny vytlačeny hydroxidem:
- C 6 H 5 SO 3 Na + 2 NaOH → C 6 H 5 ONa + Na 2 SO 3
Tato cesta byla kdysi hlavní průmyslovou cestou k fenolu.
Reakce
Fenoxid sodný je středně silná báze. Okyselením se získá fenol:
- PhOH ⇌ PhO - + H + (K = 10 −10 )
Chování kyselin a zásad je komplikováno homoasociací , což odráží asociaci fenolu a fenoxidu.
Fenoxid sodný reaguje s alkylačními činidly za vzniku alkylfenyletherů:
- NaOC 6 H 5 + RBr → ROC 6 H 5 + NaBr
Konverze je rozšířením Williamsonovy etherové syntézy . S acylačními činidly se získají fenylestery:
- NaOC 6 H 5 + RC (O) Cl → RCO 2 C 6 H 5 + NaCl
Fenoxid sodný je citlivý na určité typy elektrofilních aromatických substitucí . Reaguje například s oxidem uhličitým za vzniku 2-hydroxybenzoátu, konjugované báze kyseliny salicylové . Obecně však elektrofily nevratně útočí na centrum kyslíku ve fenoxidu.
Reference
- ^ Mezinárodní unie čisté a aplikované chemie (2014). Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 . Královská chemická společnost . s. 1071, 1129. doi : 10,1039/9781849733069 . ISBN 978-0-85404-182-4.
- ^ a b C. S. Marvel, AL Tanenbaum (1929). "y-fenoxypropylbromid". Org. Synth . 9 : 72. doi : 10,15227/orgsyn.009,0072 .Správa CS1: používá parametr autorů ( odkaz )
- ^ Kornblum, Nathan; Lurie, Arnold P. (1959). „Heterogenita jako faktor při alkylaci ambidentních aniontů: ionty fenoxidu1,2“. Journal of the American Chemical Society . 81 (11): 2705–2715. doi : 10,1021/ja01520a030 .
- ^ Michael Kunert, Eckhard Dinjus, Maria Nauck, Joachim Sieler „Struktura a reaktivita fenoxidu sodného - po průběhu Kolbe -Schmittovy reakce“ Chemische Berichte 1997 svazek 130, číslo 10, strany 1461–1465. doi : 10,1002/cber.19971301017
- ^ Smith, Michael B .; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6. ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ K. Izutsu (1990). Acidobazické disociační konstanty v dipolárních aprotických rozpouštědlech . 35 . Vědecké publikace Blackwell.
externí odkazy
![]() Média související s fenoxidem sodným na Wikimedia Commons
Média související s fenoxidem sodným na Wikimedia Commons


