Diacetát sodný - Sodium diacetate
 Diacetát sodný
|
|
| Jména | |
|---|---|
|
Název IUPAC
Diacetát sodný
|
|
| Ostatní jména
Diacetát sodný (bezvodý); Hydrogen-octan sodný; Octan sodný
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100,004,378 |
| Pletivo | diacetát sodný diacetát |
|
PubChem CID
|
|
| UNII | |
|
Řídicí panel CompTox ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| C 4 H 7 Na O 4 | |
| Molární hmotnost | 142,086 g · mol -1 |
| Vzhled | bílý prášek |
| Zápach | Vůně kyseliny octové (octa) |
| 1 g / ml | |
| Rozpustnost v alkoholu | Mírně |
| Rozpustnost v etheru | Nerozpustný |
| Nebezpečí | |
| Bezpečnostní list | PubChem sodný diacetát LCSS |
| Piktogramy GHS |
 
|
| Signální slovo GHS | Nebezpečí |
| H318 , H319 | |
| P264 , P280 , P305 + 351 + 338 , P310 , P337 + 313 | |
| inhalace hazard | Dráždivý |
| Nebezpečí očí | Dráždivý |
| Bod vzplanutí | > 150 ° C (302 ° F) |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
|
LD 50 ( střední dávka )
|
> 2 000 mg / kg (potkan, dermálně), 5 600 mg / kg (potkan, orálně) |
|
Není-li uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
| Reference Infoboxu | |
Diacetát sodný je sloučenina vzorce NaH ( C
2H
3Ó
2)
2. Jedná se o sůl z kyseliny octové . Je to bezbarvá pevná látka, která se používá v kořeních a jako antimikrobiální látka .
Příprava a struktura
Sůl se vytvoří po poloviční neutralizaci kyseliny octové, následované odpařením roztoku. Lze jej považovat za výsledek homoassociace , což je účinek, který zvyšuje kyselost kyseliny octové v koncentrovaném roztoku:
- 2 CH 3 CO 2 H + NaOH → Na + [(CH 3 CO 2 ) 2 H] - + H 2 O
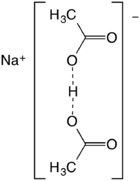
Také se popisuje jako sodná sůl kyseliny kyseliny octové, je nejlépe popsat jako sodné soli vodíku vázaného aniontu (CH 3 CO 2 ) 2 H - . Vzdálenost O ··· O je asi 2,47 angstromu . Tento druh nemá v roztoku žádnou významnou existenci, ale tvoří stabilní krystaly .
Aplikace
Jako potravinářská přídatná látka má E číslo E262 a používá se k dodání slané a octové příchuti.
Viz také
Reference
- ^ PubChem. "Diacetát sodný" . PubChem . Citováno 2019-10-24 .
- ^ a b c d e PubChem. "Diacetát sodný" . PubChem . Citováno 2019-10-24 .
- ^ Barrow, Michael J .; Currie, Murdoch; Muir, Kenneth W .; Speakman, J. Clare; White, David N, J. "Krystalové struktury některých kyselých solí monobázických kyselin. XVII. Struktura hydrogen-diacetátu sodného, znovu stanovena neutronovou difrakcí" Journal of the Chemical Society, Perkin Transaction 2: Physical Organic Chemistry 1975, str. 15- 18. doi : 10.1039 / P29750000015
- ^ Peter J. Taormina „Důsledky redukce soli a sodíku na bezpečnost mikrobiálních potravin“ v Critical Reviews in Food Science and Nutrition, 2010, sv. 50, 209-227. doi : 10,1080 / 10408391003626207
|
Acetylhalogenidy a soli octanového iontu
|
|||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | On | ||||||||||||||||||
| LiOAc |
Be (OAc) 2 BeAcOH |
B (OAc) 3 |
AcOAc ROAc |
NH 4 OAc | Ahoj | FAc | Ne | ||||||||||||
| NaOAc | Mg (OAc) 2 |
Al (OAc) 3 ALSOL AI (OAc) 2 OH Al 2 SO 4 (OAc) 4 |
Si | P | S | ClAc | Ar | ||||||||||||
| KOAc | Ca (OAc) 2 | Sc (OAc) 3 | Ti (OAc) 4 | VO (OAc) 3 |
Cr (OAc) 2 Cr (OAc) 3 |
Mn (OAc) 2 Mn (OAc) 3 |
Fe (OAc) 2 Fe (OAc) 3 |
Co (OAc) 2 , Co (OAc) 3 |
Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ga (OAc) 3 | Ge | Jako (OAc) 3 | Se | BrAc | Kr | ||
| RbOAc | Sr (OAc) 2 | Y (OAc) 3 | Zr (OAc) 4 | Pozn | Mo (OAc) 2 | Tc |
Ru (OAc) 2 Ru (OAc) 3 Ru (OAc) 4 |
Rh 2 (OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | v |
Sn (OAc) 2 Sn (OAc) 4 |
Sb (OAc) 3 | Te | IAc | Xe | ||
| CsOAc | Ba (OAc) 2 | Hf | Ta | Ž | Re | Os | Ir | Pt (OAc) 2 | Au |
Hg 2 (OAc) 2 , Hg (OAc) 2 |
TlOAc Tl (OAc) 3 |
Pb (OAc) 2 Pb (OAc) 4 |
Bi (OAc) 3 | Po | V | Rn | |||
| Fr. | Ra | Rf | Db | Sg | Bh | Hs | Mt. | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| La (OAc) 3 | Ce (OAc) x | Pr | Nd | Odpoledne | Sm (OAc) 3 | Eu (OAc) 3 | Gd (OAc) 3 | Tb | Dy (OAc) 3 | Ho (OAc) 3 | Er | Tm | Yb (OAc) 3 | Lu (OAc) 3 | |||||
| Ac | Čt | Pa | UO 2 (OAc) 2 | Np | Pu | Dopoledne | Cm | Bk | Srov | Es | Fm | Md | Ne | Lr | |||||
